| جواهر ستار التعليمية |
| أهلا وسهلا بك زائرنا الكريم ، في منتديات جواهر ستار التعليميه المرجو منك أن تقوم بتسجـيل الدخول لتقوم بالمشاركة معنا. إن لم يكن لـديك حساب بعـد ، نتشرف بدعوتك لإنشائه بالتسجيل لديـنا . سنكون سعـداء جدا بانضمامك الي اسرة المنتدى مع تحيات الإدارة |
| جواهر ستار التعليمية |
| أهلا وسهلا بك زائرنا الكريم ، في منتديات جواهر ستار التعليميه المرجو منك أن تقوم بتسجـيل الدخول لتقوم بالمشاركة معنا. إن لم يكن لـديك حساب بعـد ، نتشرف بدعوتك لإنشائه بالتسجيل لديـنا . سنكون سعـداء جدا بانضمامك الي اسرة المنتدى مع تحيات الإدارة |
 |
|  |
أهلا وسهلا بك ضيفنا الكريم، إذا كانت هذه زيارتك الأولى للمنتدى، فيرجى التكرم بزيارة صفحة التعليمــات، بالضغط هنا كما يشرفنا أن تقوم بالتسجيل بالضغط هنا إذا رغبت بالمشاركة في المنتدى، أما إذا رغبت بقراءة المواضيع والإطلاع فتفضل بزيارة القسم الذي ترغب أدناه.
 الأحد 19 يوليو - 23:43:08 الأحد 19 يوليو - 23:43:08 | المشاركة رقم: | |||||||
جوهري 
|  موضوع: الهيدروجين موضوع: الهيدروجين الهيدروجين الهيدروجين 1 - → هيدروجين ← هيليوم - ↑ H ↓ Li الجدول الدوري صفات عامة الإسم, الرقم, الرمز هيدروجين, H, 1 سلاسل كيميائية لا فلز المجموعة, الدورة, المستوى الفرعي s , 1 , 1 المظهر بدون لون كتلة ذرية 1.00794(7) g/mol شكل إلكتروني 1s1 عدد الإلكترونات لكل مستوى 1 خواص فيزيائية الحالة غاز الكثافة (0 °C) 0.0899 g/L نقطة الإنصهار 14.01 ك -259.14 م ° -434.45 ف ° نقطة الغليان 20.28 ك -252.87 م ° -423.17 ف ° حرارة الإنصهار kJ/mol (H2) 0.117 حرارة التبخر kJ/mol (H2) 0.904 السعة الحرارية (25 (H2) 28.836 C (م) ° ( J/(mol·K ضغط البخار P/Pa 1 10 100 1 k 10 k 100 k at T/K 15 20 درجة الحرارة الحرجة 32.19 K الضغط الحرج 1.315 MPa الكثافة الحرجة 30.12 g/L الخواص الذرية البنية البللورية سداسي حالة التأكسد 1 (أكسيد أمفوتيري) سالبية كهربية 2.20 (مقياس باولنج) طاقة التأين الأولي: 1312.0 kJ/mol نصف قطر ذري 25 pm نصف قطر ذري (حسابيا) 53 pm نصف القطر التساهمي 37 pm نصف قطر فان دير فال 120 pm متفرقة الترتيب المغناطيسي لا يوجد توصيل حراري (300 K ك ) 180.5 m (W/(m·K) سرعة الصوت (gas, 27 °C) 1310 m/s رقم التسجيل 1333-74-0 النظائر المهمة المقالة الرئيسية: نظائر الهيدروجين نظ ت.ط. عمر النصف طر.إ. طا.إ. MeV ن.إ. 1H 99.985% H يكون ثابت وله 0 نيوترون 2H 0.015% H يكون ثابت وله 1 نيوترون 3H متابعة 12.32 ع β- 0.019 3He المراجع الهيدرجين (الاسم مشتق من الإغريقية حيث أن هيدرو تعني ماء وجينز تعني تكون) هو عنصر كيميائي في الجدول الدوري ويرمز له بالرمز H وله الرقم الذري 1. وفي ظروف الضغط والحرارة القياسية فإنه غاز عديم اللون والرائحة, لا فلزي, وحيد التكافؤ, سريع الاشتعال, ثنائي الذرة. الهيدروجين أخف الغازات وأكثرها تواجدا في الكون. يوجد في الماء وكل المركبات العضوية والكائنات الحية. يتم تحضير الهيدروجين في المعمل عن طريق تفاعل الأحماض مع الفلزات مثل الزنك. أما لتحضير الهيدروجين بكميات كبيرة للاستخدامات الصناعية فيتم ذلك عن طريق تعديل البخار بالغاز الطبيعي. كما أن التحليل الكهربائي للماء يعتبر من الطرق البسيطة, ولكن تكاليفه عالية لدرجة عدم استخدامه تجاريا. ويحاول العلماء هذه الأيام الوصول لطرق جديدة لإنتاج الهيدروجين, وأحد هذه الطرق يتضمن استخدام الطحالب. كما أنه توجد طريقة أخرى تتضمن استخدام الجلوكوز والسوربيتول, والذي يتم في درجة حرارة منخفضة, واستخدام عامل حفاز جديد. فهرست [إظهار] 1 الخواص 2 ذرة الهيدروجين 3 استخداماته 4 تاريخ الهيدروجين 5 مستويات الطاقة الإلكترونية 6 التواجد في الطبيعة 7 مركبات الهيدروجين 8 أشكال الهيدروجين 9 النظائر 10 الاحتياطات 11 شاهد أيضا 12 المراجع 13 وصلات خارجية 14 المصادر
| |||||||
 |
| الإشارات المرجعية |
| الذين يشاهدون محتوى الموضوع الآن : 20 ( الأعضاء 3 والزوار 17) | |
|
| |
مواقع صديقة
| أعلانات نصية | |
| قوانين المنتدى | |
| إعــــــــــلان | إعــــــــــلان | إعــــــــــلان | إعــــــــــلان |

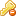 فقدت كلمة المرور؟
فقدت كلمة المرور؟ فقدت إسم العضوية؟
فقدت إسم العضوية؟












